Kitobni o'qish: «От пробирки до кастрюли: Как ученые разрабатывают продукты, которые мы едим каждый день», sahifa 2
CRISPR/Cas: как бактерии научили биологов разрезать ДНК
Все началось даже не с бактерий, а с архей – одноклеточных организмов, которые похожи на бактерии, но имеют свою эволюционную историю. Как и у бактерий, у них нет ядра, а сами они такие же маленькие, но некоторые другие характеристики архей принципиально отличаются, из-за чего в конце XX в. учеными было решено выделить их в отдельный домен. Особенностью архей считается их пристрастие жить в экстремальных условиях, например в горячих источниках и соленых озерах.
Итак, молодой докторант Университета Аликанте Франсиско Мохика, работая в маленьком городке в Испании, в 1989 г. нашел в ДНК микроскопических архей Haloferax mediterranei странные повторяющиеся 30-нуклеотидные фрагменты, разделенные неповторяющимися участками (спейсерами) примерно такой же длины. Его заинтересовала их функция. Он назвал эти участки CRISPR – clustered regularly interspaced short palindromic repeats – и начал искать похожие кластеры в ДНК других архей и бактерий. Оказалось, что CRISPR крайне распространены у прокариот. Они нашлись и у E.coli, и у других бактерий, включая патогенные виды. Следовательно, они зачем-то нужны.
После статей Мохики CRISPR начали изучать подробнее. Выяснили, что к повторам прилегают однотипные группы генов, назначение которых также неясно. Это были гены Cas – CRISPR-associated genes. И вот в 2003 г. Мохика совершает еще одно открытие: сравнивая последовательности в базах данных, он видит, что один из спейсеров CRISPR штамма кишечной палочки, устойчивой к бактериофагу P1, совпадает с ДНК этого самого фага. Мохика делает предположение, что CRISPR/Cas-система предназначена для борьбы с фагами, то есть имеет отношение к бактериальному приобретенному иммунитету. Тогда ученый не знал, какое значение имела эта догадка, но понимал, что наткнулся на нечто важное. Он написал новую статью, надеясь на публикацию в престижном издании. И хотя в Nature печатать его работу отказались, зато ее принял Journal of Molecular Evolution.
Параллельно с Мохикой над исследованием CRISPR/Cas работали и другие группы ученых. Уже через три года после его последней публикации появилось несколько работ, подтверждавших теорию Мохики по поводу функции загадочных палиндромов. А вот в действии CRISPR/Cas впервые проверили пищевые биотехнологи. Группа француза Филиппа Хорвата, пытаясь научиться эффективно отбирать сильные штаммы лактобактерий Streptococcus thermophilus для изготовления йогурта и сыра, показала, что стрептококки с большим количеством спейсерных участков в CRISPR лучше противостояли вирусам. Контролируя процесс, микробиологи заражали лабораторные стрептококки вирусами, тренируя тем самым их иммунную систему. Бактерии накапливали спейсеры и становились все более устойчивыми к фагам, что делало их эффективной основой для получения заквасок. «Криспризованный» таким образом йогурт вполне может стоять в вашем холодильнике. Он не содержит ГМО, бактерии в нем натуральные, просто их CRISPR/Cas-система натренирована лучше, чем у других. Можно считать, что они прошли полный курс профилактических прививок, а потому гораздо реже болеют12.
Эта же команда первой описала механизм работы белков Cas5 и Cas9. Интерес к феномену CRISPR возрастал. До разработки эпохальной технологии модификации генов оставалось всего ничего. В следующие несколько лет было установлено, что CRISPR/Cas – программируемая нуклеазная система, где молекула РНК, считанная с CRISPR, за счет своих спейсерных участков узнает ДНК чужеродных фагов, которые уже встречались с бактерией раньше, а прикрепленный к ней Cas-белок разрезает эту вражескую ДНК (рис. 5).
Понимание того, что CRISPR/Cas можно использовать для нарезания ДНК клеток высших организмов, пришло практически мгновенно. Стартовали множественные эксперименты по ее использованию. На базе природных систем стали создавать упрощенные искусственные конструкции, включающие белок-киллер Cas9. Наконец в 2012 г. две женщины-биолога, Эмманюэль Шарпантье и Дженнифер Дудна, разработали рабочую инженерную систему CRISPR/Cas9 (через восемь лет они получат за нее Нобелевскую премию)13, а генная инженерия преобразилась.
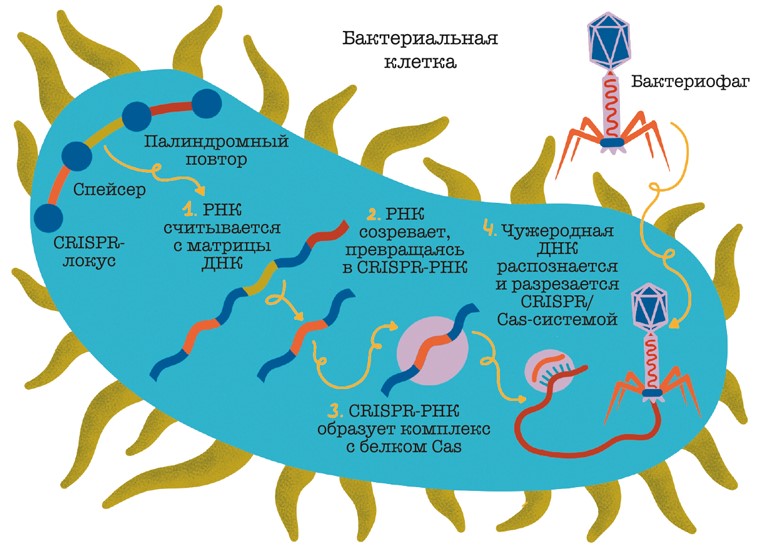
Рис. 5. Принцип работы защитного CRISPR/Cas-механизма бактерии при попадании в клетку бактериофага
При помощи CRISPR/Cas9 стало возможным успешно проводить все виды модификаций генома: вносить точечные мутации, встраивать, исправлять, заменять или удалять крупные ДНК-последовательности и фрагменты выбранных генов (рис. 6).
Сегодня CRISPR/Cas9 и родственные ей усовершенствованные системы применяются во множестве лабораторий и компаний. Уже опубликованы сотни результатов работ, проводимых с применением CRISPR, описаны десятки удачных экспериментов по редактированию геномов дрожжей, растений, насекомых и животных. С помощью генетических ножниц, например, были внесены точные модификации в геномы пшеницы и табака, получены новые сорта риса14. Больше того, на базе этой технологии уже существует первое лекарство для людей – Casgevy. Оно лечит серповидноклеточную анемию, редактируя сломанный ген в предшественниках красных стволовых телец – гемопоэтических стволовых клетках. После лечения клетки начинают производить полноценный гемоглобин вместо аномального, характерного для болезни.
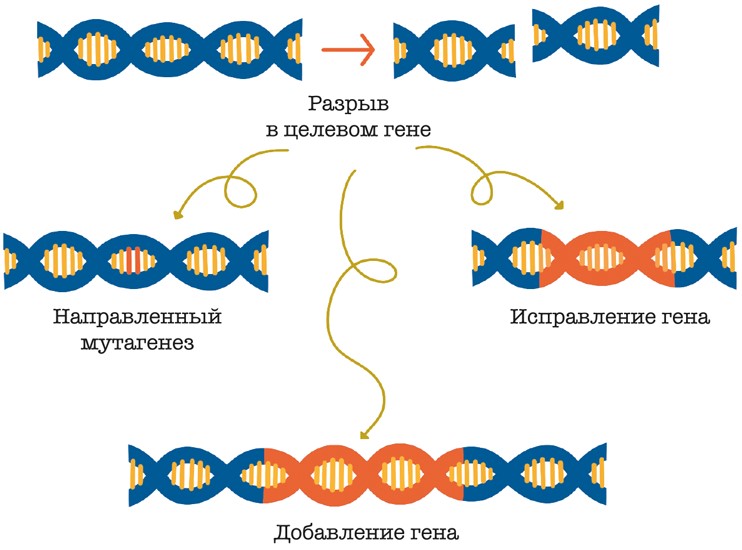
Рис. 6. Виды различных воздействий, проводимых с помощью CRISPR/Cas9-конструкции
С приходом CRISPR риск неспецифического воздействия на ДНК пусть и не исчез совсем, но крайне минимизировался. Следовательно, безопасность методов генной инженерии вышла на новый уровень. Использование CRISPR/Cas не идет ни в какое сравнение с предыдущими поколениями нуклеаз, не говоря уже о ненаправленном мутагенезе или соматической гибридизации, когда клетки двух разных растений просто заставляют слипнуться, перетасовывая их гены в надежде получить удачный гибрид. Это все равно что дать одному противнику в руки пушку, а другому – пинцет.
Кроме того, что изменились сами методы редактирования генома, эволюционировал и подход к получению ГМ-продуктов. С новыми возможностями степень измененности ГМ-растений постепенно начала снижаться. Теперь далеко не все они – «франкенфуд» с генами из далеких друг от друга организмов, вроде помидоров с генами камбалы, которые в свое время наделали много шума в сети (эта разработка компании DNA Plant Technology до рынка так и не добралась, а сама компания обанкротилась)15. Многие ГМ-сорта включают гены из других растений, что уже не выглядит столь кощунственно, но и тут уровень вмешательства разнится. Взять, например, рис с генами кукурузы. Скрестить эти два растения невозможно, а потому перенос генов кукурузы в рис называется трансгенезом – это когда в организм переносят чужеродные для него гены, которые не могли бы оказаться в нем натуральным путем. Но часто ученые добавляют в свои сорта гены из родственных видов. Это уже организмы не трансгенные, а цисгенные. Так, в Швеции разработали картофель, не подверженный картофельной гнили благодаря встраиванию генов из диких видов картофеля, устойчивых к этому заболеванию16. Нередки также случаи, когда в ДНК растения вставляют копии его собственных генов или меняют не гены, а вспомогательные участки, отвечающие за активность считывания генетической информации. Это позволяет усиливать определенные признаки – например, способность накапливать витамины в листьях или, наоборот, устранять либо сводить к минимуму нежелательные свойства, такие как горечь у горчичной зелени17.
Остаются еще общественные опасения по поводу влияния ГМ-растений на биосферу, но до сегодняшнего дня все они беспочвенны. Если следовать существующим рекомендациям, в частности не высаживать модифицированные виды в центрах происхождения их диких родственников, вытеснить другие растения из их ареалов они не смогут. Новые сорта с измененным геномом «успешны» не потому, что агрессивны или отличаются инвазивностью, а потому, что приносят пользу человеку: удобны в выращивании, питательны, неприхотливы и т. д. Поэтому, даже если зеленые ГМО и выйдут за пределы полей, они, скорее всего, просто займут свою скромную нишу наряду с другими растениями. Экологические риски при этом рассчитываются для каждого нового ГМ-сорта. Все промышленные биоинженерные растения подвергаются мониторингу, за ними долго наблюдают, проверяя, вредят ли они другим сортам и видам, насекомым или почвенным микроорганизмам. И пока результаты всех подобных экспериментов не дают повода для беспокойства18.
К тому же сами компании, продающие ГМ-семена, совершенно не склонны выпускать их «на волю». Чтобы фермеры не могли сами запасать семенной материал и находились в зависимости от биотех-гигантов, в США при поддержке Министерства сельского хозяйства еще в 1990-е гг. была разработана технология «терминатор», или GURT – genetic use restriction technology19. Ее идея в том, чтобы сделать семена «одноразовыми». В их ДНК вшита последовательность-предохранитель, которая не дает привнесенным генам считываться. И вырезается эта последовательность только после обработки специфическим биологическим веществом-активатором, которое наносят на семена перед продажей. Если посадить такие растения и попытаться их размножить, плоды появятся, но особенностей генетически модифицированного сорта не сохранят. Другая разновидность GURT еще радикальнее: при ее использовании семена в растениях получаются стерильными – из них вообще ничего нельзя вырастить.
Хотя «терминатор» призван в том числе контролировать распространение генетически модифицированных посадок, на Monsanto и ее коллег в связи с GURT, когда метод только появился, обрушилось немало критики. Он был воспринят как проявление беспрецедентной жадности со стороны больших корпораций. В то же время стоит признать, что покупка обычных F1-гибридов мало чем отличается от использования «терминатора». При желании семена гибридов первого поколения можно прорастить, но, согласно второму закону Менделя, они не дадут потомков с устойчивыми сортовыми качествами: наследственные признаки расщепятся, перемешаются и результат не сможет удовлетворить ни одного растениевода.
То, что ГМО меняются и становятся все более изученными и понятными, неизбежно влияет на рынок. Постепенно даже с учетом живучести укрепившихся негативных стереотипов отношение к сельскохозяйственным ГМ-растениям на уровне правительств становится все более лояльным. При оценке безопасности новых сортов регуляторы начинают исходить не из технологии их создания, а из состава продуктов. Если в растении нет ничего вредного и оно не синтезирует несвойственных ему чужеродных белков – значит, и контролировать его не нужно. Согласно обновленному законодательству в США, Канаде, Австралии, Японии, Китае и ряде других стран к продуктам редактирования, в которые не вносились чужеродные гены, больше не применяются ограничения, актуальные для трансгенов20. То есть, если из генома растения всего лишь удален ненужный ген или произведена небольшая замена нуклеотидов, ГМ-растением оно не считается21.
Где-то ослабление законов происходит быстро, где-то – медленно. В некоторых государствах, включая Россию, законы довольно строги. Выращивать ГМ-культуры в нашей стране можно только на опытных участках, а для ввоза разрешены лишь отдельные линии модифицированных растений (всего 28), среди которых кукуруза, картофель, соя, сахарная свекла и рис. Чтобы получить допуск на ввоз, сорта проходят проверку: их безопасность исследуют на крысах в течение полугода.
В результате такой разницы в запретах примерно 98% всех ГМ-растений выращивается всего в 10 странах. Этот перекос, с одной стороны, выгоден государствам, активно развивающим генетическую селекцию, а с другой – позволяет остальным регионам искать собственные точки роста. В частности, Россия, дав ГМО зеленый свет, могла бы заработать на экспорте ГМ-картофеля или пшеницы, тем более что российскими учеными уже разработан картофель, устойчивый к колорадскому жуку22. Но пока этого не произошло, наш рынок остается привлекательным для органик-производителей.
Эпигенетика: как повлиять на ДНК, не разрезая ее
Одним из самых молодых направлений работы для селекционеров стали подходы эпигенетики – науки об управлении работой генов23. Дело тут в том, что производство белков внутри клеток зависит не только от самой ДНК, но и от множества других факторов. Это значит, что свойства организмов могут меняться даже тогда, когда их ДНК остается прежней, а меняется лишь эффективность ее считывания. Конечно, ученым хочется овладеть методами такого влияния на геном. Это даст возможность получать лучшие образцы растений без изменения последовательности нуклеотидов в ДНК.
Как это работает? Представим, что вам нужно перед экзаменом повторить конспект, но времени у вас на это пять минут, не больше. За такой срок все лекции никак не прочесть, поэтому вам остается сосредоточиться на главном – на тех абзацах, что вы сами выделили маркером или красивой закладкой. Так и живая клетка производит те белки, чьи гены открыты для считывания. Только «закладками» в ее конспекте служат не цветные наклейки, а, например, метильные группы (CH3–), и отмечает она ими не самое важное, а то, что читать не нужно24. Когда ДНК метилируется, обзаводясь новыми «украшениями» в виде CH3-групп, фермент, отвечающий за постройку мРНК, не узнает ее и не может найти начало кода, откуда следует читать. А нет мРНК – нет и белка. Получается, что ген есть, но он как бы выключен.
Метилирование ДНК у растений и животных – вполне естественный процесс. И что интересно, он не всегда работает как выключатель. Иногда после метилирования определенных участков генома синтез белков, наоборот, резко возрастает (тогда молекулярная «закладка» работает так же, как и бумажная: помогает найти нужную строчку). Люди и это научились использовать: изменяя метилирование ДНК, можно увеличить активность генов, отвечающих за производство растением запасных белков, в том числе увеличить «белковость» зерна пшеницы. Снижение уровня метилирования приводит также к наследуемому признаку карликовости у риса. Карликовый рис хорош тем, что не прилегает к земле.
Теперь предположим, что ген у нас вполне рабочий. Но и тут совсем не обязательно его прочтение закончится синтезом белка. Как мы помним, превращение последовательности ДНК в белок – это своеобразная система двойного шифрования: на основе ДНК сперва создается молекула матричной РНК, а уже она становится образцом для сборки протеина. И вот эта матричная РНК может быть разрушена в цитоплазме клетки до того, как ею воспользуются25. Называют это явление посттранскрипционным молчанием (ген замолкает уже после того, как произошла транскрипция – изготовление клеткой мРНК). Эта ситуация часто возникает сама по себе, когда ученые привносят в ДНК растений дополнительные гены. ДНК меняется, но вставленный ген не работает – его продукт разрушается, не дойдя до состояния готовности. Впервые молчание генов у генетически измененных организмов описали еще в 1990 г. Тогда введение в геном петунии дополнительных генов, отвечающих за красную окраску цветков, неожиданно снизило количество красного пигмента в растении.
Казалось бы, для селекционера в этом нет никакой выгоды. Но затем выяснилось, что посттранскрипционное молчание можно использовать для создания растений, устойчивых к растительным вирусам. Тогда механизм замолкания генов будет направлен против чуждых растению вирусных мРНК. А если заставить молчать те гены, которые производят ненужные белки, получатся новые перспективные сорта. Используя механизмы разрушения мРНК, можно снизить в кофе содержание кофеина26, а в табаке – никотина27. Есть и более амбициозные проекты. Например, генетики испанского Института сельского хозяйства в Кордове смогли почти полностью очистить пшеницу от глиадина – компонента глютена, из-за которого у некоторых людей возникает иммунная реакция.
Нужно сказать, что, когда биологи прибегают к посттранскрипционному молчанию, они обычно используют и CRISPR/Cas9. То есть чуть-чуть изменить ДНК растений все же приходится28. Например, чтобы целевая мРНК разрушалась, на нее можно натравить уже присутствующие в растениях для собственных нужд малые интерферирующие РНК. За их производство отвечают некодирующие участки генома, которые и подвергаются доработке. Как мы увидим дальше, генетики вообще любят использовать не один, а несколько инструментов сразу.
Что еще могут геномные технологии
Несмотря на то что селекция за последние 30 лет сильно изменилась, в ней используются и традиционные методы получения новых сортов или растений с нужными характеристиками. Только теперь они сосуществуют с геномными технологиями.
Взять хотя бы прививку. Это давно известный способ размножения растений, с которым повсеместно сталкиваются садоводы-любители. В ходе прививки стебель одного растения – привой – пересаживают на корень или стебель другого – подвой (рис. 7).

Рис. 7. Прививка растения
Главное – соединить части растений так, чтобы их ткани плотно прилегали друг к другу. Тогда со временем они срастутся и из нескольких разных растений получится одно.
Используют прививку чаще всего для того, чтобы объединить свойства двух разных видов. Как правило, привой от культурного растения с хорошими плодами соединяют с подвоем дикой разновидности, которая гораздо более устойчива к различным болезням и вредителям. Или, если в саду мало места, можно привить к одной яблоне ветки разных сортов и даже ветку груши. Тогда садовод будет собирать с одного дерева разные плоды.
И все же главной задачей прививки остается улучшение здоровья культурных насаждений. Так, в конце XIX в. прививка помогла сберечь европейские сорта винограда от нашествия филлоксеры – микроскопической тли, поедающей виноградные корни. Ее завезли в Европу из Северной Америки. Местные виноградари долго не могли понять, отчего страдают их хозяйства. Только в 1868 г. вредитель был установлен. Но мало было найти тлю – требовалось ее обезвредить. Тем более что нашествие филлоксеры по масштабам было нешуточное. Каждая тля может за раз отложить до 800 яиц, а за сезон насекомое воспроизводится пять-шесть раз. Выдержать такой натиск могли далеко не все, многие виноградники погибли.
Долгое время попытки бороться с филлоксерой оставались безуспешными. Не помогали ни протравление почв, ни временное затопление ферм. Отрасль испытывала большие трудности и вполне могла бы не оправиться от удара, если бы не идея привить европейский культурный виноград Vitis vinifera на дикий североамериканский – Vitis labrusca, давно знакомый с вредителем, а потому устойчивый к нему29. Тактика оказалась крайне эффективной и до сих пор остается единственным действенным способом избавиться от виноградной тли, не считая разве что посадок в районах с песчаными почвами. Хорошо защищены от филлоксеры не только привитые сорта, но и гибриды, имеющие виноград Vitis labrusca в родителях. Один из них, «изабелла», очень популярен в домашних хозяйствах в России и в жарких странах. Он неприхотлив и отлично растет как в холодном, так и в тропическом климате. А вот в Европе продажа вин из «изабеллы» запрещена везде, кроме Швейцарии. Официальная причина – излишнее количество токсичного метанола, накапливающееся в них в ходе брожения. Есть, однако, мнение, что правительство ЕС, запретив «изабеллу», пошло на уступки местному винодельческому лобби, которое боялось конкуренции и было заинтересовано в продвижении своих классических сортов.
Иногда результат прививки очень похож на ГМО. Например, в одной из серий мультсериала «Симпсоны» Гомер занимался разведением «томака» – генетических помидоров-мутантов, содержащих никотин30. При этом растения томата практически с такими же свойствами были получены в США в 2003 г. – путем прививания. Пробы показали наличие в «томаке» никотина, но не в плодах, а в листьях31.
Казалось бы, если ДНК подвоя и привоя в ходе прививки не меняется, почему химический состав привоя может измениться? Все просто. Привой и подвой, сливаясь в единый организм, обмениваются веществами друг с другом. Поэтому, если вы привили ветку скороспелой яблони к позднеспелому сорту, срок созревания привоя может заметно сдвинуться. Не исключено, что изменятся также другие характеристики: сила роста или размер плодов.
Для прививки можно использовать и генетически измененный подвой. При этом технически плоды с таких растений не будут ГМО, ведь их ДНК останется такой же, как была, а все новые признаки не станут наследоваться при размножении семенами. Метод прижился в одном из самых востребованных направлений, где геномные технологии проявляют себя во всей красе. Это fast-track breeding, или ускоренное скрещивание.
Подходы этой категории призваны сокращать сроки селекции тех культур, цикл размножения которых чересчур долог. Только подумайте: чтобы дерево дало плоды, его нужно выращивать несколько лет32. Это означает, что после получения каждого гибрида селекционер вынужден годами ждать хотя бы того, чтобы можно было оценить результат работы. А если потребуется провести еще несколько последовательных скрещиваний, выведение нового сорта может занять и 30 лет.
Чтобы исправить положение, как нельзя лучше подходит прививка на ГМ-подвой с усиленно вырабатываемыми генами цветения. Тогда из корневища к листьям будут поступать специфические белки, запускающие механизм взросления, и привой начнет цвести гораздо быстрее (рис. 8Б).
Чуть более радикальный способ приблизить сроки цветения и плодоношения, тем самым ускорив получение нового сорта, – изменить ДНК растения, но лишь временно (рис. 8А). Ген быстрого цветения можно ввести в исходный сорт, а на последнем этапе селекции – вывести. Для этого используют возвратное скрещивание, когда гибрид объединяют с родительским растением.

Рис. 8. Различные методики скрещивания растений: А – использование ускоренного и возвратного скрещиваний для получения устойчивого к заболеванию гибрида; Б – прививка на ГМ-растение
Наконец, сократить время работы селекционерам помогает простое умение читать ДНК. Анализируя геном молодых ростков, можно не ждать, когда те повзрослеют и дадут урожай, а сразу отбирать лучшие. А чтобы понять, насколько растение устойчиво к патогену или гербициду, необязательно проводить полевые испытания, достаточно просто подтвердить наличие нужных элементов генома в пророщенном семечке.
Селекцию, при которой растения выбираются исходя из их генетических показателей, называют маркер-вспомогательной, потому что главную роль в ней играют короткие последовательности ДНК – молекулярные маркеры, наследуемые вместе с ценными признаками. Ученые берут у растений небольшой образец листа, ищут эти маркеры и затем делают выводы о наличии или отсутствии у них ценных признаков в будущем. Сейчас это уже рутина. А в последние годы, со снижением цен на маркерное детектирование, площадь применения такой технологии расширилась еще больше. Теперь ее используют не только для создания новых сортов, но и для определения качества семян. Например, фермеры могут сдать в лабораторию новый семенной материал и проверить его принадлежность к дорогим элитным сортам. Или же проанализировать собственные семена, прошедшие несколько циклов культивирования, чтобы оценить степень расщепления генов (снова вспоминаем второй закон Менделя) и понять, можно ли их сажать снова без потери урожая.
Получается, даже если оставить в стороне ГМО, геномные технологии все глубже внедряются в сельское хозяйство. От секвенирования (расшифровки) ДНК отдельных организмов ученые со временем перешли к сбору и анализу данных о геномах множества растений одного вида или разных сортов. Эти данные, в свою очередь, сравниваются с результатами анализа транскриптомов – всех синтезируемых организмами мРНК, протеомов – всех белков, метаболомов – всех метаболитов. Объемы обрабатываемой информации растут, а методы работы совершенствуются.
Такой комплексный подход в перспективе поможет еще больше узнать о хранении и передаче генетической информации у растений. Перед селекционерами стоят важные задачи33. Во-первых, они хотят научиться предсказывать урожайность новых сортов и их реакции на внешние стрессы. Умея прогнозировать, человек сможет разрабатывать растения для использования в будущем, скажем, через 50 лет, когда климат станет более жарким, изменятся ареалы насекомых и животных, появятся новые фитопатогены34. Перспективы выращивания известных растений пересматривают уже сейчас. Так, многим специалистам злаком будущего представляется сорго. Оно способно добывать воду из глубоких слоев почвы и экономить влагу, что делает его чрезвычайно засухоустойчивым. К тому же сорго не привередливо к почвам и отлично растет на жаре.
Во-вторых, сегодня все чаще говорят о новом витке одомашнивания диких видов. Идея в том, чтобы выбрать наиболее приспособленные и живучие и заново вывести из них культуры, дающие вкусные плоды и большой урожай35. В процессе селекции мы раз за разом выбирали одни варианты растений, упуская из виду другие, которые теперь могли бы пригодиться. Вернувшись к геномам диких предков тех растений, с которыми мы работаем сейчас, можно найти более удачные генетические вариации с точки зрения устойчивости сортов к экстремальным температурам или засухам36.
В любом случае геномные технологии продолжат и дальше менять растениеводство. Даже если люди вдруг откажутся от генетической инженерии и запретят всю модифицированную сою, у ученых останется еще очень много забот. Хотя такой вариант развития событий маловероятен. Создание новых сортов с измененной ДНК – слишком заманчивая идея, от которой трудно отказаться. Тем более что генная инженерия порой оказывается единственным выходом для решения насущных проблем рынка. Однажды она уже спасла гавайскую папайю, а в скором времени ее помощь может понадобиться и другим фруктам. На Филиппинах в ближайшие годы, вероятно, начнут расти генетически измененные бананы, устойчивые к опасной болезни Tropical race 4, вызываемой грибком Fusarium oxysporum f. sp cubense. В 2023 г. разработавшая их компания Tropic Biosciences из Великобритании уже прошла одобрение в этой стране с другим продуктом – бананом, который не темнеет во время хранения37. Апельсины в будущем тоже могут получить улучшенную ДНК. Индустрии пригодятся сорта, невосприимчивые к гринингу – бактериальной инфекции, из-за которой плоды цитрусовых не вызревают, оставаясь маленькими, зелеными и слишком горькими, чтобы продавать их в розницу. Зеленые апельсины опадают с больных деревьев, которые теряют листья, плохо растут, а через несколько лет после заражения и вовсе погибают. В США фермеры называют грининг убийцей апельсинов. Во Флориде объемы их производства упали на 75% с 2005 г., когда инфекция была зарегистрирована там впервые. Страдают от грининга сады и в других регионах: в Бразилии, Юго-Восточной Африке, Индии и Китае, где о нем было известно с начала прошлого века. Заболевание распространяется с насекомыми-листоблошками, а эффективных способов лечения посадок по-прежнему нет (хотя есть методы сдерживания, например, с помощью инъекций антибиотиков).
